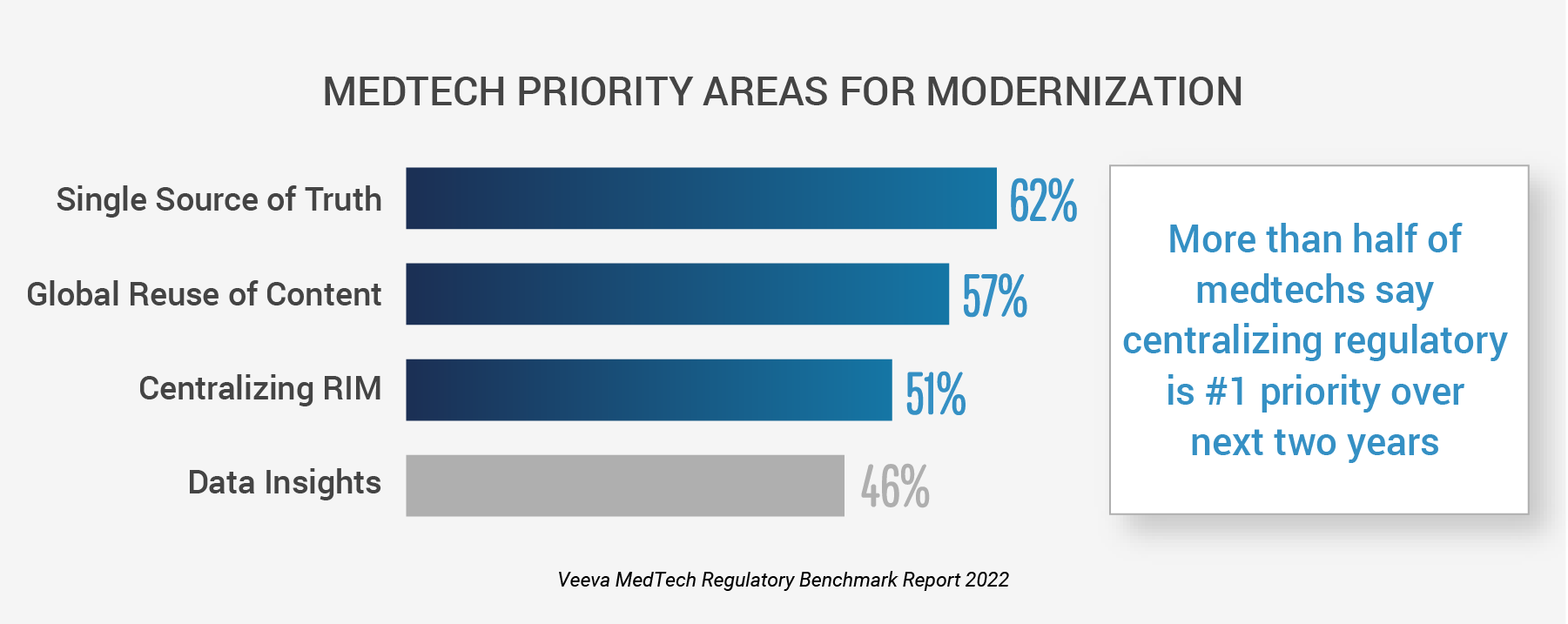
Un’indagine rivela che la massima priorità per il settore Medtech è la necessità di centralizzare la regolamentazione. La crescente necessità di ottenere visibilità e immediatezza favorisce il passaggio ai sistemi normativi digitali
Secondo il Veeva MedTech Regulatory Benchmark Report, le aziende del settore medtech stanno adottando misure per migliorare la regolamentazione. Più della metà delle aziende afferma che la creazione di un’unica fonte di informazioni normative (62%) e l’implementazione di un sistema globale e centralizzato di gestione (RIM) (51%) saranno i principali obiettivi per i prossimi due anni.
Con la modernizzazione del RIM in corso, i responsabili del settore medtech stanno mettendo insieme dati, contenuti e sistemi per migliorare gli insight e il time to market.
Perché scegliere la tecnologia normativa digitale
Due aziende su cinque hanno già scelto la tecnologia normativa digital; questo cambio verso sistemi RIM evidenzia la necessità di una maggiore trasparenza e collaborazione tra i team locali, per soddisfare l’evoluzione delle normative e i requisiti di change management.
Il rapporto rivela cambiamenti positivi negli aspetti normativi e margini di miglioramento in alcuni ambiti.
Persistono i processi manuali: solo il 13% delle aziende ha implementato un sistema RIM digitale globale per la gestione end-to-end delle operazioni regolatorie. Molte organizzazioni medtech si affidano a processi manuali, a fonti di dati scollegate e a sistemi frammentati (che non sono scalabili); rendendo più difficile l’espansione in nuovi mercati.
La fonte unica per i dati di registrazione è in crescita: le aziende che raccolgono i dati di registrazione globali in un unico sistema stanno aumentando di anno in anno; evidenziando l’urgenza di creare un’unica fonte per le informazioni normative.
I processi di compliance post-market mancano di collegamenti: la maggior parte delle aziende (83%) dispone di integrazioni parziali, soluzioni puntuali o processi manuali tra i settori normativo e della qualità per acquisire le modifiche post-vendita all’interno del portafoglio prodotti. La mancanza di un processo di controllo continuo e automatizzato aumenta i rischi e può portare a problemi di compliance o ritardi.

Processi piú fluidi per condividere dati di alta qualità tra teams
L’introduzione di nuove normative e l’aumento della complessità della supply chain, ha portato le aziende del settore a valutare metodi piú fluidi.
Necessari per condividere dati di alta qualità tra i vari team“, ha dichiarato Seth Goldenberg, Vice President di Veeva MedTech.
“Questa ricerca dimostra che il settore medtech sta compiendo progressi, migliorando le operazioni normative per una migliore visibilità globale, l’accuratezza dei dati e la conformità“.
Il Veeva MedTech Regulatory Benchmark Report esamina i progressi del settore dei dispositivi medici e diagnostici verso la modernizzazione delle operazioni regolatorie. I partecipanti all’indagine sono professionisti degli affari regolatori di oltre 100 organizzazioni medtech in tutto il mondo, dalle multinazionali alle medie imprese. Lo studio annuale completo analizza come le aziende medtech gestiscono la compliance e la visibilità a livello globale; la velocità di commercializzazione; la conformità post-market e la modernizzazione.